臨床前動(dòng)物實(shí)驗(yàn)方案盡可能模擬臨床設(shè)計(jì)和使用。應(yīng)當(dāng)確認(rèn)在輸送,、植入或使用器械中的所有步驟,,并制定每一個(gè)步驟的可接受標(biāo)準(zhǔn)。建議對(duì)每個(gè)驗(yàn)收標(biāo)準(zhǔn)應(yīng)用半客觀的評(píng)定量化表(例如李克特量表,,Likert scale),。如果器械與輔助設(shè)備一同輸送或使用,,則可接受標(biāo)準(zhǔn)應(yīng)包含評(píng)估系統(tǒng)相容性的要素。評(píng)級(jí)標(biāo)準(zhǔn)應(yīng)當(dāng)囊括從器械準(zhǔn)備到放置或使用乃至取回和重新放置過(guò)程中的所有步驟,。如果器械通過(guò)手術(shù)放置,,則應(yīng)描述器械從進(jìn)入體壁到比較終器械操作期間的所有步驟。中成藥臨床前動(dòng)物實(shí)驗(yàn)外包,;福建高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?/p>

英國(guó)學(xué)者對(duì)人體試驗(yàn)與臨床前動(dòng)物實(shí)驗(yàn)結(jié)果差異的新解釋:2007年1月25日,來(lái)自英國(guó)倫敦帝國(guó)學(xué)院,、倫敦國(guó)王學(xué)院和Babraham研究所的學(xué)者在法國(guó)一個(gè)移植會(huì)議上提出,人體的記憶T細(xì)胞(實(shí)驗(yàn)動(dòng)物體內(nèi)不存在)可能是造成TGN1412Ⅰ期臨床試驗(yàn)志愿者多組織功能衰竭的關(guān)鍵因素。大約50%的人體T細(xì)胞是記憶細(xì)胞,即它們?cè)谌说囊簧幸蚝图膊〉纫蛩卦?jīng)被,。然而,動(dòng)物模型,比如用于TGN1412臨床前研究的動(dòng)物,卻沒(méi)有這么多數(shù)量的記憶T細(xì)胞,這是因?yàn)闉榱祟A(yù)防感染,這些動(dòng)物一直被置于無(wú)菌環(huán)境下飼養(yǎng),。江西臨床前動(dòng)物實(shí)驗(yàn)檢測(cè)化學(xué)藥臨床前動(dòng)物實(shí)驗(yàn)機(jī)構(gòu);
醫(yī)療器械臨床前動(dòng)物實(shí)驗(yàn)的主要目的是研究它的安全性,;生物相容性是醫(yī)療器械安全性的特征之一(如血液相容性,、細(xì)胞毒性);有效性不是臨床前評(píng)價(jià)的主要方向,,但是包含了一定程度的有效性內(nèi)容,;建立適當(dāng)?shù)哪P停行缘难芯靠梢宰鳛榕R床前評(píng)價(jià)的重要內(nèi)容,,即試驗(yàn)器械的實(shí)際使用情況和預(yù)期用途的符合性,但是,,這種研究結(jié)果不能作為醫(yī)療器械有效性評(píng)價(jià)的客觀證據(jù),,只能作為是否可轉(zhuǎn)入人體進(jìn)行臨床研究的輔助參考。有效性的客觀研究是不切合實(shí)際的,,有時(shí)候一定要在動(dòng)物實(shí)驗(yàn)中驗(yàn)證醫(yī)療器械有效性只是廠家的一廂情愿,。但是也有例外,如結(jié)構(gòu)性心臟病類器械,、血管疾病類器械和止血材料等可在某種程度上得到驗(yàn)證,。無(wú)論怎樣設(shè)計(jì)試驗(yàn)?zāi)P停c器械預(yù)期使用的人體對(duì)象存在較大的差異,;設(shè)計(jì)和完成一種完全符合或近似預(yù)期使用人體對(duì)象的動(dòng)物模型難以實(shí)現(xiàn),;醫(yī)療器械臨床研究才是其有效性驗(yàn)證的關(guān)鍵階段,也是安全性的另一驗(yàn)證(確證)階段,。
關(guān)于臨床前動(dòng)物實(shí)驗(yàn),,資料顯示,截至2012年7月,,衛(wèi)生部干細(xì)胞整頓工作辦公室的調(diào)查結(jié)果是——干細(xì)胞已經(jīng)在我國(guó)300家左右的醫(yī)院,、機(jī)構(gòu)開(kāi)展。而國(guó)家干細(xì)胞工程技術(shù)研究中心主任,、中國(guó)醫(yī)學(xué)科學(xué)院血液學(xué)研究所研究員韓忠朝認(rèn)為,,300家醫(yī)療機(jī)構(gòu)是個(gè)保守的數(shù)字,,“這是衛(wèi)生部開(kāi)展的一個(gè)自查,自己報(bào)上的有300家,,還有沒(méi)有報(bào)上去的呢,?實(shí)際肯定不止300家做”。事實(shí)上,,除了造血干細(xì)胞血液疾病以外,,衛(wèi)生部沒(méi)有批準(zhǔn)任何一家醫(yī)療機(jī)構(gòu)用干細(xì)胞臨床任何一種疾病,全球的絕大多數(shù)干細(xì)胞研究都在臨床前動(dòng)物實(shí)驗(yàn)或臨床階段,,只有加拿大在2012年5月份批準(zhǔn)了美國(guó)一家公司生產(chǎn)的干細(xì)胞藥物用于移植物抗宿主病,、日本iPS細(xì)胞實(shí)驗(yàn)自去年來(lái)得到**支持。英瀚斯專業(yè)做生物藥臨床前動(dòng)物實(shí)驗(yàn)外包,。
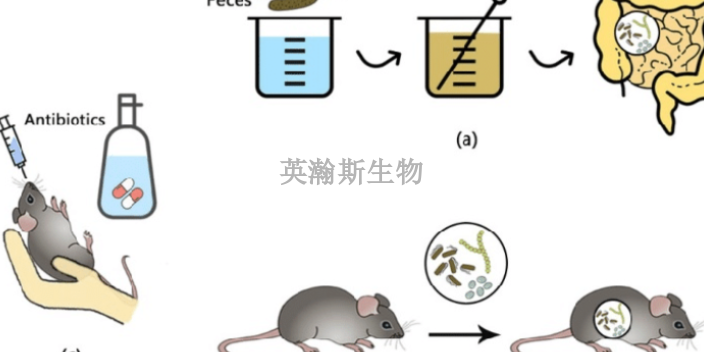
關(guān)于臨床前動(dòng)物實(shí)驗(yàn)的故事,。過(guò)去十余年,國(guó)內(nèi)某團(tuán)隊(duì)也一直致力于理想的“超級(jí)疫苗”研究,,基于已有的研究基礎(chǔ),,在此次**科研攻關(guān)中,他們?cè)O(shè)計(jì)出新的疫苗抗原分子,,建立哺乳動(dòng)物細(xì)胞表達(dá)系并純化了抗原蛋白,,用微劑量免疫動(dòng)物后(小動(dòng)物5微克,大動(dòng)物10微克),,產(chǎn)生了高達(dá)百萬(wàn)倍試紙測(cè)試效價(jià)的抗體,。免疫抗體經(jīng)在國(guó)家批準(zhǔn)的P3實(shí)驗(yàn)室測(cè)定,中和病毒的效價(jià)都達(dá)到了要求,,有的超過(guò)了檢測(cè)單位設(shè)定的比較高限,。目前,他們已開(kāi)始進(jìn)行臨床前動(dòng)物實(shí)驗(yàn),,在免疫猴子,、小鼠和雪貂準(zhǔn)備攻毒中和實(shí)驗(yàn)。中成藥臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液??湖北值得信賴臨床前動(dòng)物實(shí)驗(yàn)研究
生物藥臨床前動(dòng)物實(shí)驗(yàn)指標(biāo),;福建高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?/p>
臨床前動(dòng)物實(shí)驗(yàn)的計(jì)劃和實(shí)驗(yàn)方案制定:首先,臨床前動(dòng)物實(shí)驗(yàn)研究必須經(jīng)過(guò)周密計(jì)劃,。為此,,實(shí)驗(yàn)計(jì)劃需要有一定資質(zhì)的機(jī)構(gòu)或者個(gè)人提出,由有適當(dāng)資質(zhì)和經(jīng)驗(yàn)的指定的專題負(fù)責(zé)人進(jìn)行指導(dǎo),。專題負(fù)責(zé)人宜在實(shí)驗(yàn)場(chǎng)所辦公,,便于指導(dǎo)和監(jiān)督實(shí)驗(yàn)技術(shù)的實(shí)施。專題負(fù)責(zé)人負(fù)責(zé)研究結(jié)果的解釋、分析,、形成文件和報(bào)告,。實(shí)驗(yàn)方案應(yīng)包括《藥物非臨床研究質(zhì)量管理規(guī)范》第八章第二十九條中所要求的適用于一般GLP方案的十五項(xiàng)要素,并宜包含如特殊環(huán)境下的研究規(guī)范(操作指南),。任何**終已通過(guò)的實(shí)驗(yàn)方案的改變和修改以及修改原因都必須經(jīng)由專題負(fù)責(zé)人簽字并簽署日期,。實(shí)驗(yàn)方案和任何修改必須提供給質(zhì)量保證部門檢查。研究開(kāi)始前需要先通過(guò)動(dòng)物倫理委員會(huì)對(duì)已確定的實(shí)驗(yàn)方案進(jìn)行審批,。福建高質(zhì)量臨床前動(dòng)物實(shí)驗(yàn)?zāi)募液?/p>



